Biomolecular electronics

Responsabile: Prof.ssa Marta De Zotti, PA, Dipartimento di Scienze Chimiche
Composizione del GRE:
- Marta De Zotti, PA
Aree di ricerca di afferenza:
Attività:
Peptidi in dispositivi biomolecolari. Il mondo dipende in modo cruciale dai dispositivi elettronici che, a loro volta, si basano sul trasporto elettronico. In Natura, i processi di trasferimento di elettroni sono della massima importanza ed eseguiti magistralmente: basti pensare agli enzimi o alla fotosintesi. Pertanto, lo sviluppo di dispositivi elettronici basati esclusivamente su biomolecole[i] è altamente auspicabile, dati gli evidenti risparmi economici e guadagni ambientali che questa rivoluzione comporterebbe. Tuttavia, le biomolecole hanno spesso poca utilità al di fuori del loro ambiente naturale. Le proteine, materiali molto promettenti per le applicazioni bioelettroniche, spesso sono troppo instabili al di fuori del loro ambiente biologico per essere davvero utili. Il DNA mostra una buona conduttività solo per brevi distanze, dopodiché diventa un isolante. In collaborazione con la Dott.ssa Emanuela Gatto dell’Università di Tor Vergata, abbiamo sviluppato un minuscolo dispositivo interamente formato da molecole biologiche autoassemblate, che riesce a convertire la luce in corrente elettrica con un’efficienza maggiore di altri sistemi simili ma “non bio” e stabile per mesi[ii]. Cuore del sistema è un analogo di un peptide naturale chiamato tricogina GA IV, sintetizzato dal fungo trichoderma logibrachiatum[iii].
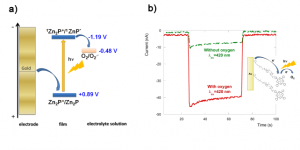 Tricogina appartiene alla famiglia dei peptaibolici, che sono peptidi naturali che possiedono strutture elicoidali ben definite, notevolmente stabili in condizioni ambientali estreme. La caratteristica che rende questo “peptide bionico” interessante è la sua capacità di agire come filo elettrico, mediando efficacemente il trasferimento elettronico. Applicando un approccio bioispirato basato sull’associazione delle basi azotate complementari del DNA adenina e timina, abbiamo dato al peptide la capacità di auto-organizzarsi su un elettrodo d’oro in fili molecolari. Con lo stesso metodo, si è legato tramite l’interazione tra basi azotate complementari una porfirina, in grado di trasformare la luce in corrente elettrica.
Tricogina appartiene alla famiglia dei peptaibolici, che sono peptidi naturali che possiedono strutture elicoidali ben definite, notevolmente stabili in condizioni ambientali estreme. La caratteristica che rende questo “peptide bionico” interessante è la sua capacità di agire come filo elettrico, mediando efficacemente il trasferimento elettronico. Applicando un approccio bioispirato basato sull’associazione delle basi azotate complementari del DNA adenina e timina, abbiamo dato al peptide la capacità di auto-organizzarsi su un elettrodo d’oro in fili molecolari. Con lo stesso metodo, si è legato tramite l’interazione tra basi azotate complementari una porfirina, in grado di trasformare la luce in corrente elettrica.
Questi fili molecolari sono stati caratterizzati da tecniche elettrochimiche e spettroscopiche e si sono dimostrati molto stabili nel tempo, conservando la loro attività per molte settimane. Sotto illuminazione, il sistema completamente formato da biomolecole si è dimostrato in grado di generare corrente con un’efficienza superiore a quella registrata in sistemi simili non “bio”.
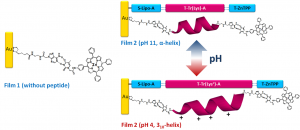 L’analogo della tricogina in esame possiede residui carichi positivamente: facendo fluire sul sistema ancorato all’elettrodo d’oro alternativamente soluzioni a pH 4 o 11, il peptide passa reversibilmente da una conformazione elicoidale 310 ad una α. A questo cambio conformazionale corrisponde un aumento di efficienza del processo di generazione della fotocorrente. In futuro potremo quindi progettare moduli complessi autoassemblati, in grado di convertire la luce incidente in corrente elettrica, ad efficienza modulabile[iv].
L’analogo della tricogina in esame possiede residui carichi positivamente: facendo fluire sul sistema ancorato all’elettrodo d’oro alternativamente soluzioni a pH 4 o 11, il peptide passa reversibilmente da una conformazione elicoidale 310 ad una α. A questo cambio conformazionale corrisponde un aumento di efficienza del processo di generazione della fotocorrente. In futuro potremo quindi progettare moduli complessi autoassemblati, in grado di convertire la luce incidente in corrente elettrica, ad efficienza modulabile[iv].
[[i]] P. Facci, Biomolecular electronics, Elsevier Ed., 2014.
[[ii]] E. Gatto, S. Kubitzky, M. Schriever, S. Cesaroni, C. Mazzuca, G. Marafon, M. Venanzi, M.
De Zotti, Angew. Chem. Int. Ed., 2019, 58, 7308.
[[iii]] Auvin-Guette C., Rebuffat S., Prigent Y., Bodo B., J. Am. Chem. Soc., 114, 2170-2174 (1992).
[[iv]] S. Kubitzky, M. Venanzi, B. Biondi, R. Lettieri, M. De Zotti, E. Gatto, Chem. Eur. J., 2020, in press. DOI: 10.1002/chem.202004527
Peptides in biomolecular devices. The world depends crucially on electronic devices that, in turn, rely on charge transport. In Nature, electron transfer (ET) processes are of the utmost importance and wonderfully performed: just think of enzymes or the photosynthesis. Therefore, the development of electronic devices based on biomolecules1 is highly desirable, considering the high gain in terms of both economic and environmental impact. However, biomolecules have often little use outside their natural environment. Proteins, very promising materials for bioelectronic applications, are often too unstable outside their biological environment to be truly useful. DNA shows good conductivity only for short distances, after which it becomes an insulator. In collaboration with Dr. Emanuela Gatto of the University of Tor Vergata, we have developed a tiny device entirely made up of self-assembled biological molecules, which is able to convert light into electric current with greater efficiency than other similar but “non-bio” systems. “and stable for months2. At the core of the system there is an analog of a natural peptide called trichogin GA IV, synthesized by the fungus Trichoderma logibrachiatum3. Trichogin belongs to the family of peptaibols, which are natural peptides that possess well-defined helical structures, remarkably stable in extreme environmental conditions. The feature that makes this “bionic peptide” interesting is its ability to act as an electric wire, effectively mediating electron transfer. By applying a bioinspired approach based on the association of the complementary nitrogenous bases of DNA adenine and thymine, we gave the peptide the ability to self-organize on a gold electrode in molecular strands. With the same method, a porphyrin, capable of transforming light into electric current, was linked through the interaction between complementary nitrogenous bases. These molecular threads have been characterized by electrochemical and spectroscopic techniques and have proved to be very stable over time, maintaining their activity for many weeks. Under illumination, the system completely formed by biomolecules proved capable of generating current with a higher efficiency than that recorded in similar non “bio” systems.
The trichogin analog has positively charged residues in its sequence: by alternately flowing on the system – anchored to the gold electrode – solutions at pH 4 or 11, the peptide reversibly passes from a 310– to a α-helical conformation. This conformational change corresponds to an increase in the efficiency of the photocurrent generation process. In the future we will be able to design complex self-assembled modules, capable of converting incident light into electric current, with tunable efficiency4.
REFERENCES
[[1]] P. Facci, Biomolecular electronics, Elsevier Ed., 2014.
[[2]] E. Gatto, S. Kubitzky, M. Schriever, S. Cesaroni, C. Mazzuca, G. Marafon, M. Venanzi, M.
De Zotti, Angew. Chem. Int. Ed., 2019, 58, 7308.
[[3]] Auvin-Guette C., Rebuffat S., Prigent Y., Bodo B., J. Am. Chem. Soc., 114, 2170-2174 (1992).
[[4]] S. Kubitzky, M. Venanzi, B. Biondi, R. Lettieri, M. De Zotti, E. Gatto, Chem. Eur. J., 2020, in press. DOI: 10.1002/chem.202004527
Elenco delle ultime cinque pubblicazioni:
- Kubitzky S., Venanzi M., Biondi B., Lettieri R., De Zotti M.*, Gatto E., A pH-induced reversible conformational switch able to control the photocurrent efficiency in a peptide supramolecular system. Chem. Eur. J., 2020, in press. DOI: 10.1002/chem.202004527
- Bertran A., Henbest K.B., De Zotti M., Gobbo M., Timmel C.R., Di Valentin M., Bowen A.M., Light-induced triplet−triplet electron resonance spectroscopy. J. Phys. Chem. Lett., 2020, in press. DOI: 10.1021/acs.jpclett.0c02884
- De Zotti M., Corvi G., Gatto E., Di Napoli B., Mazzuca C., Palleschi A., Placidi E., Biondi B, Crisma M., Formaggio F., Toniolo C., Venanzi M., Controlling the formation of peptide films: fully developed helical peptides are required to obtain a homogenous coating over a large area. ChemPlusChem, 84,1688-1696 (2019).
- Gatto E., Kubitzky S., Schriever M., Cesaroni S., Mazzuca C., Marafon G., Venanzi M., De Zotti M.*, Building supramolecular DNA-inspired nanowires on gold surface: from 2D to 3D. Angew. Chem. Int. Ed., 58, 7308-7312 (2019).
- De Zotti M.*, Syryamina V.N., Hussain R., Longo E., Siligardi G., Dzuba S.A., Stella L., Formaggio F., A temperature-driven, reversible helical handedness inversion in peptaibol analogs tuned by the C-terminal capping moiety. ChemBioChem, 20, 2125-2132 (2019). COVER ARTICLE.
Contatti:
Dipartimento di Scienze Chimiche, Universita’ di Padova, via Marzolo 1, I-35131 Padova, email: marta.dezotti@unipd.it, tel. +390498275280, sito web del gruppo: http://wwwdisc.chimica.unipd.it/marta.dezotti/
Laboratorio del Dipartimento di Scienze Chimiche


- Il gruppo di ricerca di Marta De Zotti opera presso il Dipartimento di Scienze Chimiche. Ha a disposizione un laboratorio attrezzato per la sintesi organica e un laboratorio in cui sono collocate le sue strumentazioni per la purificazione e caratterizzazione dei prodotti, in condivisione con altri gruppi di ricerca. Il gruppo di ricerca è specializzato nella sintesi, purificazione, studio ed applicazione di peptidi contenenti amminoacidi stericamente ingombrati. Tra gli strumenti in dotazione al gruppo di ricerca si annoverano due sintetizzatori semiautomatici di peptidi Biotage, una HPLC preparativa, una HPLC analitica e due strumenti per la purificazione in media pressione Biotage Isolera Prime.






